技術・研究材料紹介(企業広告)
抗体医薬品バイオアナリシスのための前処理法
日本ウォーターズ株式会社 佐々木俊哉
【はじめに】
新薬開発が高分子バイオ医薬品へシフトを始めている現在,ペプチド医薬品やタンパク医薬品などの迅速で高感度なPK/PD 解析手法が必要とされている.従来から使われているイムノアッセイ法は優れた手法であるが,アッセイ法開発に時間とコストがかかる,再現性に乏しい,交叉反応他の課題があり,低分子医薬品の定量に日常的に使用されているLC-MSの適用が望まれている.ここでは生体中の抗体医薬品をLC-MSで高感度定量する場合の酵素消化を含む前処理法に焦点をあて解説する.
【抗体医薬品のLC-MSバイオアナリシスワークフロー】
生体試料,例えば血清中の抗体医薬品をLC-MSで定量する方法には種々のアプローチがある.抗体医薬品をintactの状態で高感度に定量できると理想的であるが,生体中には大量の内因性抗体が存在し,その中から測定対象を分離し,かつ高感度にMS検出することは簡単ではない.最近注目され,実用化されている手法のひとつに,ターゲットとなる抗体医薬品をトリプシン等の酵素で消化し,得られる消化ペプチドの中から,マトリックス中の内因性タンパク質およびペプチドの消化ペプチドに無い配列のペプチド(特異的ペプチド,unique peptides)をみつけ,測定することにより定量する方法がある.この手法は簡易で迅速な優れた手法であるが,酵素消化の最適化,消化効率の補正,消化ペプチドの精製などの課題がある.
【酵素消化の最適化,消化効率の補正】
ターゲットモデルとして乳がんの分子標的治療薬である抗体医薬品trastuzumabを用い酵素消化の最適化と消化効率の補正について検討を行った.はじめにtrastuzumabをトリプシン消化して得られるC末端がリジン(L)およびアルギニン(R)であるペプチドでヒトの内因性タンパク質から生成しないunique peptidesの探索を行い,HC領域の3種のペプチドと2種のLC領域ペプチドを選択した.これら5種のペプチドについてLC-MS/MSにてMRM測定を行い,シグナル強度が強く安定しているHC領域のペプチド2種(T3, T9)をトレース用のsignature peptidesとした.更にsignature peptidesのN末あるいはC末にリジンまたはアルギニンを介して配列を拡張したextended peptidesを同位体標識したものを合成し,内標準とした(Fig.1).これらを用いて,タンパク可溶化試薬RapiGestSFで変性後,還元アルキル化を行い,トリプシン消化を行った.トリプシン消化の最適化を検討し,最適条件において実際のtrastuzumabから得られるT3, T9ペプチドと,そのextended peptidesの消化効率に相関があり,補正に使用できることが確認された(Fig.2, 3).
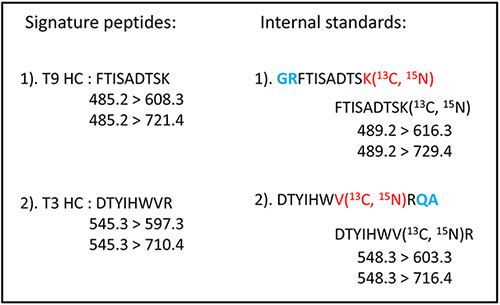
Fig.1 選択したSignature Peptides と 内標準 (13C15N-isotopically labeled extended peptides)
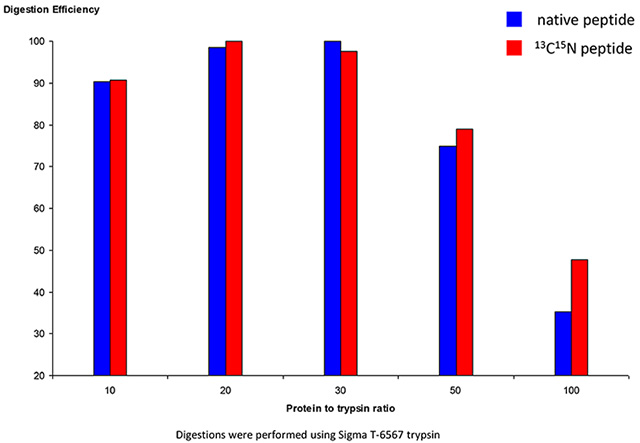
Fig.2 トリプシン消化条件の最適化 : タンパク / トリプシン比(w/w)
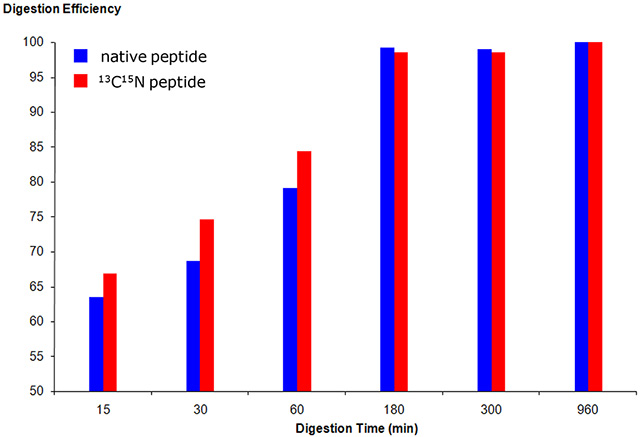
Fig.3 トリプシン消化条件の最適化 : 消化時間
【血清中トリプシン消化ペプチドの精製】
生体中には大量の内因性ペプチド,タンパク質が存在し,またリン脂質や塩なども高濃度に含まれている.LC-MSで高感度定量を行うためには,サンプル前処理によりこれらのマトリックス成分から分析種であるペプチドを精製する必要がある.
Fig.4に分子標的型抗体医薬品trastuzumabを添加した血清のトリプシン消化ペプチドをそのままLC-MS/MSで分析した場合 と,イオン交換-逆相ミックスモード固相で精製を行ってから分析した場合の比較例を示す.ミックスモード固相で精製を行うことにより,大幅なシグナル強度向上とバックグラウンドノイズの削減が達成されている.Fig.5に本ワークフローの全体を示す.
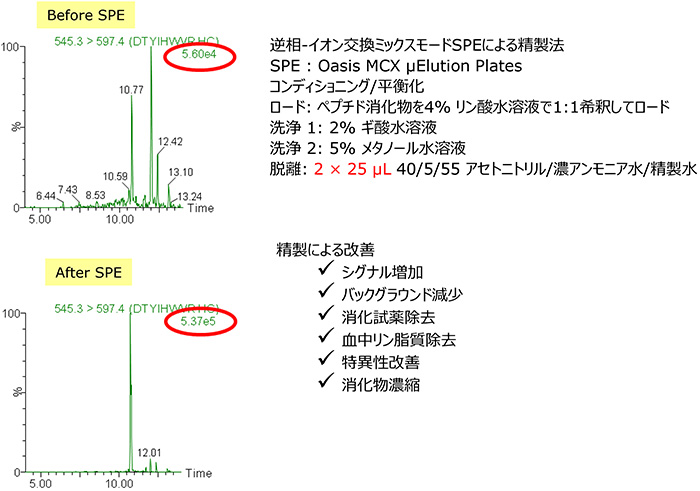
Fig.4 trastuzumab添加血清消化物のクリーンアップ例 : 逆相-イオン交換ミックスモード固相
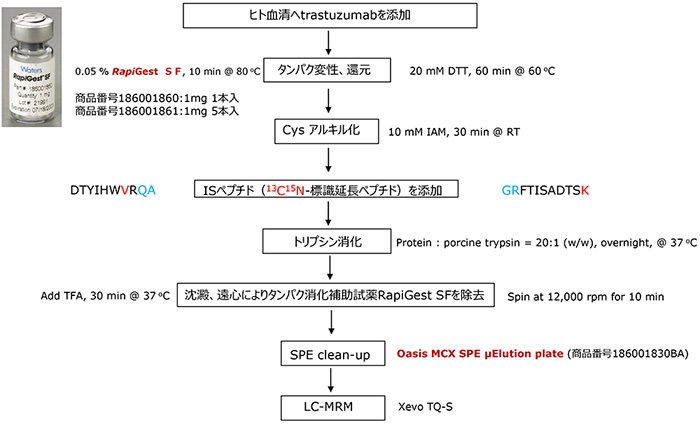
Fig.5 生体中抗体医薬品 trastuzumabサンプル前処理ワークフロー
【おわりに】
抗体医薬品の高感度バイオアナリシスを実現するためには本発表で示したサンプル前処理だけではなく,LC分離とMSを含む全てに渡って注意深く考慮する必要がある.注意深く最適化された場合,本アプローチによりng/mLオーダーでの定量を高精度に実施することが可能となる.
【参考文献】
- Catalin Doneanu, Hua Yang, Paul Rainville, Ed Bouvie, and Robert Plumb, Optimization of Trypsin Digestion for MRM Quantification of Therapeutic Proteins in Serum, Waters Application Note 720004507EN, 2012
- Generic Protein and Peptide Level Sample Preparation for Protein Bioanalysis, Waters Technology Brief 720004442EN, 2012
