受賞者からのコメント
 |
創薬貢献・奨励賞を受賞して大塚製薬株式会社
|
はじめに
この度は,「Robotics,IT,機械学習及び計算化学を用いた創薬スクリーニング基盤研究」という題目で令和5年度創薬貢献・奨励賞を賜りました.この大変名誉ある賞をいただき,身に余る光栄です.日本薬物動態学会役員,選考委員会の先生方,ならびに本賞にご推薦くださいました大塚製薬株式会社 樫山英二博士に厚く御礼申し上げます.私はこれまでの研究生活の中でin silicoを活用した研究に取り組んでまいりました.誠に僭越ながら,以下で私の研究について,ご紹介をさせて頂きます.
研究内容
新薬の誕生確率は約3万分の一といわれています.日々多くの候補化合物が合成されており,そのすべての化合物に対してADME試験を実施することは不可能に近いと考えられます.ゆえに,マンパワーやコストとプロジェクトのステージや優先度を加味して,ADME試験を実施していくこととなります.勿論,評価する化合物数や試験項目数が多いにこしたことはありませんが,多くなりすぎることで試験作業に時間を取られ,数値を出すことが目的化し,化合物のADME評価やヒト予測が疎かになれば元も子もありませんので,評価する化合物数や試験項目数を一定数に絞らざるをえません.そこで,この部分を補う手段の一つとして,“in silico”技術があげられます.
薬物動態学会の会員の皆様には釈迦に説法でありますが,シトクロムP450(CYP)は,多様な形態で存在し,内因性基質(例えば,アンドロゲンやエストロゲン)の酸化に重要な役割を果たし,生物機能制御を行っています(Sasahara et al., The Journal of Neuroscience, 27:7408(2007)).また,薬物に対しても同様の役割を果たしています(Sasahara et al., Drug Metabolism and Disposition, 43:1267(2015)).実際,CYPは約75%の薬物代謝反応の触媒として関与しており,最も重要な薬物代謝酵素です.その中でもCYP2D6はCYPによる代謝で2番目に重要なCYP分子種です.チオリダジンはフェノチアジン型抗精神病薬の一つで,ドパミンD2受容体拮抗活性を示します.チオリダジンはクロルプロマジンなどの他のフェノチアジン型抗精神病薬と比べて独特の代謝プロファイルを示します.具体的には,フェノチアジン環に結合した硫黄原子が主にCYP2D6により優先的に酸化され,2-スルホキシドが主要な代謝産物となり,興味深いことにこの代謝産物はチオリダジンよりもドパミンD2受容体に対する活性が強いことが明らかになっています.一方,この代謝産物の形成は臨床使用に多くの深刻な問題を引き起こすことがわかっています.したがって,薬物のCYP代謝のプロファイルとメカニズムを明らかにすることが重要です.これまでにWangらはチオリダジンとCYP2D6の結晶構造を明らかにしています(Journal of Biological Chemistry, 287:10834 (2012)及びJournal of Biological Chemistry, 290:5092(2015)).私は,まずチオリダジンのin vitroでの代謝特性をLC-UV-MS/MSで体系的に明らかにし,分子動力学法 (MD)及び密度汎関数法 (DFT)を用いて結晶結合ポーズと代謝物との対応を調べ,代謝機構を原子・電子レベルで明らかにしました.その結果,CYP2D6の反応中心での基質の配向が代謝反応に極めて重要であることを示しました(Sasahara et al., Bioorganic & Medicinal Chemistry, 23:5459(2015)).本研究で用いたアプローチや方法はCYPによる薬物代謝の一般的な非経験的予測法の構築にもつながることが期待されています.
それに加え,私はスループット性の高い機械学習にも着目し,薬物動態予測モデルを構築しました.CYP3A4阻害試験を例に予測モデルの構築方法及び検討内容を紹介します.社内約16,000,社外約14,000の合計約30,000化合物を用いて,様々な分類器や特徴量を用いて予測モデルを検討しました.4つの分類器(Deep learning,XGBoost,Random forest,Support vector machine)の中で,XGBoostは予測性能が良く,予測モデル内がブラックボックスにならない(結果までの判断のプロセスや重要な記述子情報などの情報取得が可能)ことから,第一選択にすべき分類器と判断しました(Sasahara et al., Drug Metabolism and Pharmacokinetics, 39:100395(2021)).CYP阻害での構築法に準じ,CYP阻害のみならず,代謝安定性,膜透過性,タンパク結合,P-gp基質性,BCRP基質性などの他の薬物動態試験に対する精度の高い予測モデルも構築しています.
機械学習は万能ではなく,外挿性の問題があることがわかりました.社内化合物といえども,創薬時に合成される化合物は予測モデルにとって外挿になる場合もあります.その場合,無理に予測結果を表示するのではなく,予測困難であることを示す必要があります.つまり予測する化合物が外挿か内挿か,いわゆる予測の信頼性を評価する手段が必要です.そこで上述した予測モデルの出力結果に対して,さらにRandom forest法を用いて別の機械学習モデル(信頼性評価モデル)を構築しました.特徴量には信頼性に影響を及ぼすと考えられる記述子を中心に用い,教師データには予測モデルから出力された予測結果を用いました.代謝安定性予測モデルの予測結果の信頼性を高,中,低の3段階に分類し,各正答率を調べたところ,信頼度と正答率に良好な相関が認められたことから,これを信頼性評価モデルとすることができると判断しました(Sasahara et al., Drug Metabolism and Pharmacokinetics, 39:100395(2021)).
さらに構造的に活性な部位を表示する機械学習モデルも構築しました.約30,000の社内化合物のin vitro代謝安定性試験の結果を用いて,活性部位を表示する様々な種類の機械学習モデルを構築しました.その中の一部の予測モデルで予測された自社化合物の代謝部位は,実験的に同定された代謝活性部位と一致し,代謝部位の正答率(予測/実数)は90%以上でした.これらのモデルは,複数のスクリーニングプロジェクトを通して高精度でした.構造上の活性部位を示すことで,合成前に対応する部分構造を変更することができます.その結果,創薬スクリーニングを加速することが期待されます(Sasahara et al., Drug Metabolism and Pharmacokinetics, 39:100401(2021)).
この様に分子動力学法,量子化学計算や機械学習など様々なin silico技術を用いて,創薬プロセスを迅速化できる手法を研究してきました.もちろんこれらは試験結果を予測できるという強みがあります.それに加えて,そのメカニズム,つまり構造上でのキーとなる活性部位を理解することができます.その為,合成デザインでピンポイントに構造変換ができるという強みもあります.
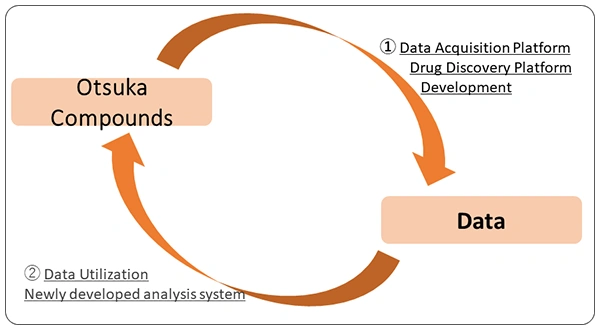
近年,初期探索試験(CYP阻害,代謝安定性,各種トランスポーター試験)を高度にオートメーション化する取り組みに従事しました.それは各創薬プロジェクトからの依頼から試験結果の登録・利活用まで(全部署で利用する共通試験依頼システム→化合物プレート作成依頼・管理→前処理ロボット→分析機器 (LCMS)→自動クロマト解析→自動パラメータ算出→自動データ解析(データサイエンス)→結果表示→データ登録)を高度に自動化するというものです.その際も,本研究での経験を活かし,図1の様なプラットフォームとシステムを構築しました.
おわりに
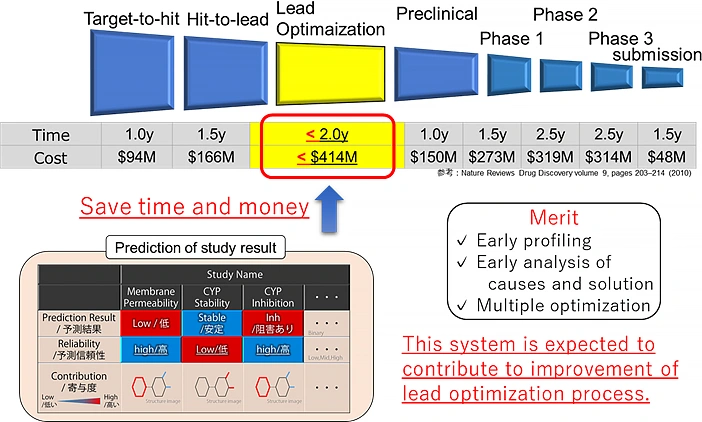
この様に私はin silicoを用いて様々な研究を行ってきました.この強みを活かして,患者さん,そして会社の為に,より良い新薬の上市への一助となれるように引き続き尽力してまいる所存です(図2).
最後になりましたが,私に研究のいろはをご指導頂いた故・筒井和義 広島大学名誉教授,浮穴和義 広島大学教授,博士研究に際しご指導くださいました中馬 寛 徳島大学名誉教授に厚く御礼申し上げます.大塚製薬株式会社入社後,ご指導・ご支援を頂きました樫山英二博士,竹内健二博士,笹邉裕行博士,鈴木智樹博士,柴田昌和博士,植松直也博士,稲葉智也様,同僚の皆様に,この場をお借りしまして深く感謝申し上げます.




